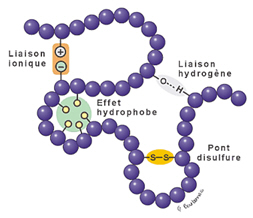
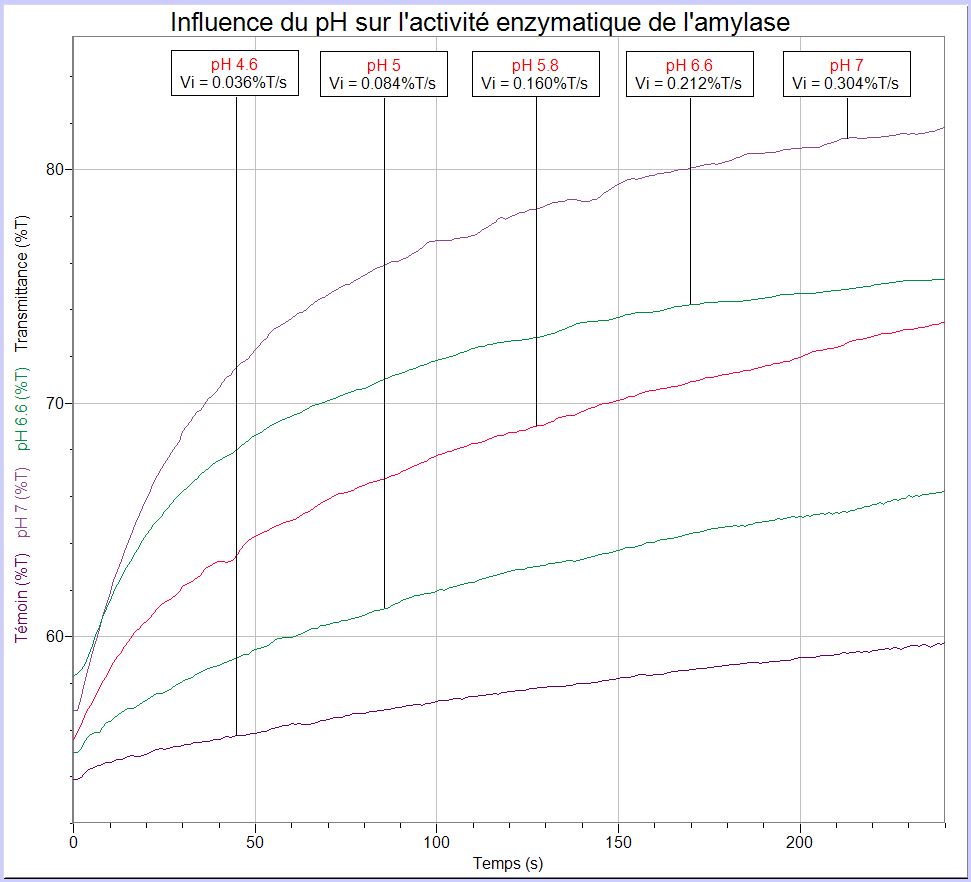
Interprétation :
Les enzymes sont des protéines, des macromolécules composées d'acides aminés. Ces acides aminés portent des charges ioniques. Les variations de pH modifient les charges ioniques des acides aminés, ce qui entraine la modification de la forme de la protéine. Si la forme du site actif de l'enzyme est modifié, la catalyse enzymatique peut-être ralentie et même bloquée.
Protocole :
- Régler le colorimètre sur 565 nm.
- Remplir une cuve avec de leau distillée, l'insérer dans le colorimètre et appuyer sur "CAL" pour faire le zéro.
- Introduire 3,5 mL de solution d'amidon dans une cuve puis ajouter 3 gouttes d'eau iodée et mélanger.
- Au dernier moment, introduire 0.3 mL de solution d'amylase, mélanger et mettre la cuve dans le colorimètre.
- Attendre que la valeur de la transmittance se stabilise (environ 2-3 sesondes).
- Lancer la mesure.
- Une fois l'acquisition terminée, stocker la courbe obtenue.
- Faire de même pour chaque solution de pH différent.
- Ajuster l'échelle.
- Utiliser la fonction "droite de régression" du logiciel sur les parties pertinentes des courbes pour connaître les vitesses initiales de la catalyse enzymatique.
- Annoter la courbe et mettre un titre.
- Ranger le poste de travail.
Principe :
L'amylase est une enzyme spécifique de l'amidon. Elle catalyse l'hydrolyse de ce dernier. Une solution d'amidon se colore en bleu en présence d'eau iodée. L'hydrolyse de l'amidon par l'amylase entraîne la décoloration de la solution.Nous pouvons donc étudier ce phénomène par colorimétrie.
Nous allons étudier l'influence du pH sur l'activité enzymatique de l'amylase.
- Mélanger l'empois d'amidon avec les différentes solutions tampons :
100 mL d'empois d'amidon / 250 mL de solution tampon
- Réserver les solutions d'amidon ainsi obtenues au bain-marie à 37°C
Remarque : ne pas réaliser de solutions basiques car l'eau iodée ne se fixe pas sur l'amidon en milieu basique.
| pH | Acétate de sodium (en mL) | Acide acétique (en mL) |
| 4.2 | 24 | 76 |
| 4.6 | 45 | 55 |
| 5 | 68 | 32 |
| 5.4 | 83 | 17 |
| | Phosphate disodique (en mL) | Phosphate monosodique (en mL) |
| 5.8 | 8 | 92 |
| 6.2 | 18.6 | 81.4 |
| 6.6 | 37.5 | 62.5 |
| 7 | 61.1 | 38.9 |
Matériel :
- Colorimètre + cuves
- Pipettes (ou seringues) + propipette
- Eau iodée
- Solution d'amylase : 4 cachets (sans enrobage) de Maxilase pour 100 mL d'eau distillée
- Empois d'amidon à différents pH :
1- Préparer un empois d'amidon à 1% (10 g/L)
2- Préparer les solutions nécessaires à la fabrication de solutions tampons acétate / acide acétique et de tampon phosphate monosodique / phosphate disodique :
- acétate de sodium à 0.2 mol/L (16.4 g/L d'acétate de sodium anhydre)
- acide acétique à 0.2 mol/L (11.58 mL/L d'eau distillée)
- hydrogénophosphate disodique à 0.1 mol/L (14.2 g/L d'hydrogénophosphate disodique anhydre)
- dihydrogénophosphate de sodium à 0.1 mol/L (15.6 g/L de dihydrogénophosphate de sodium, 2H2O)
3- Réaliser des solutions tampons à différents pH :